英语原文共 11 页,剩余内容已隐藏,支付完成后下载完整资料
一种富Sn的Au-Sn钎料薄膜的简单电沉积工艺
摘要:Au-Sn系统中富Sn共晶合金(90wt%Sn)为富Au共晶合金(20wt%Sn)提供了一种潜在的较为廉价的替代,该种合金可用于光电子及微机电系统设备封装,同时也可能作为一种无铅钎料用于微电子封装。含有可达到这一目的的共晶成分的富Sn的Au-Sn钎料薄膜可以通过一种简单的电沉积工艺来制备。电解液由氯化锡和柠檬酸铵的一种溶液组成。向电解液中加入单质金有两种方法,可以加入由柠檬酸钠制备的Au纳米颗粒(lt;20nm)悬浮液,也可以直接添加Au粉(直径为500-800nm的颗粒物)。生成的悬浮液可用于电沉积共晶及近共晶合金薄膜。通过后一种方式可以获得均匀的厚度和成分,也即直接添加Au粉。沉积物中的含金量随着溶于电解液中的Au颗粒的增多以及电流密度的增大而增大。室温时效会导致AuSn4形成于Au颗粒-Sn基体的界面。具有近共晶成分的沉积物的回流会引起Sn和AuSn4这两种共晶相的形成。
- 引言
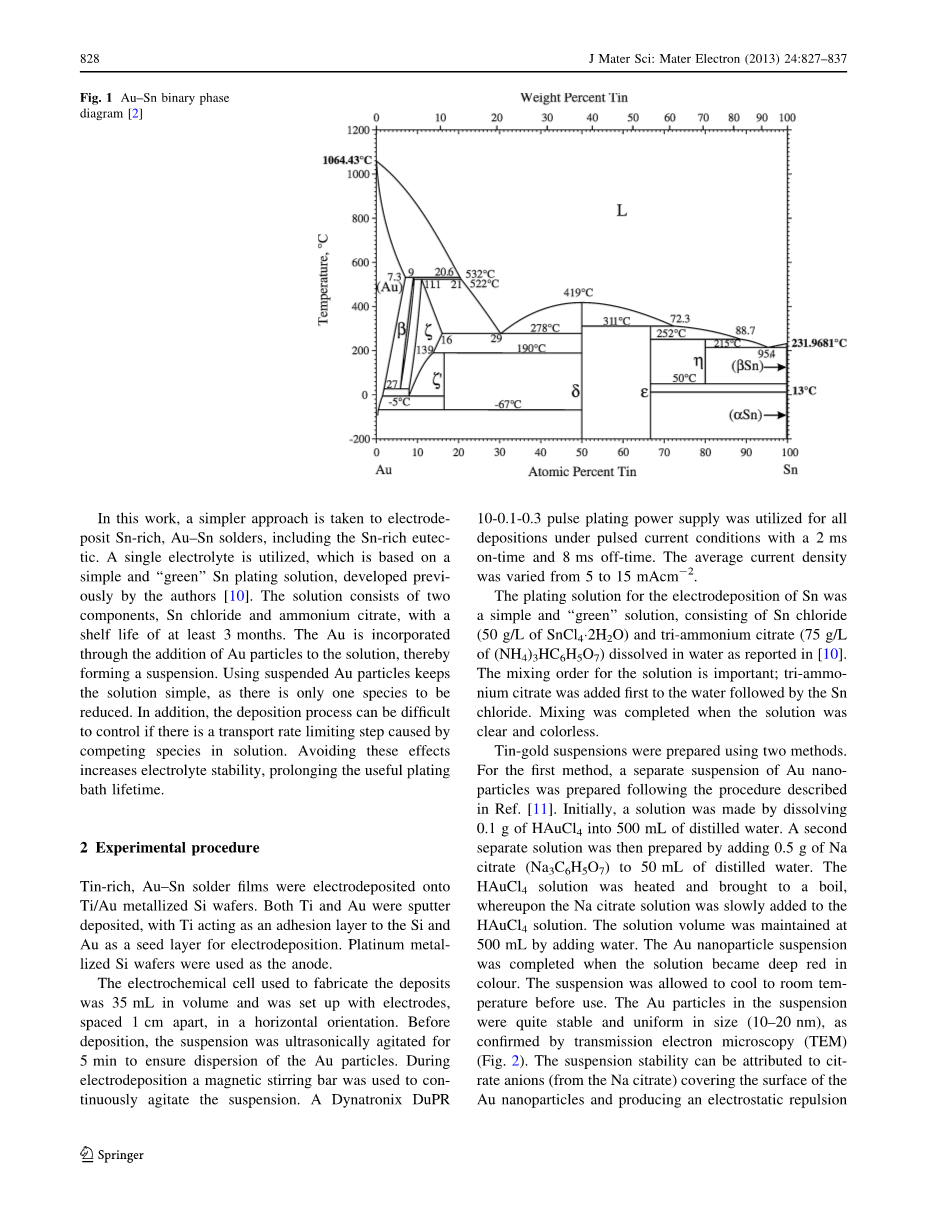
Au-Sn共晶合金钎料被广泛用于光电子设备及微机电系统(MEMS)的封装[1]。Au-Sn相图(图1)中有两种共晶合金,其中一种为含20wt%Sn(30at%Sn)的富Au合金,其低共熔温度为280℃,另一种则为含90wt%Sn(93.2at%Sn)的富Sn合金,其低共熔温度为217℃。行业标准为前一种共晶合金,它被认为是一种较硬的钎料,并且有着力学性能和热性能的优良组合[1]。富Sn的共晶合金化合物是一种潜在的价格较低的替代,因其熔点(217℃) 相对较低[1,3],也有望作为一种无铅钎料用于微电子设备中。然而,富Sn的共晶合金也存在着一些局限性。具体而言,富Sn的Au-Sn合金容易氧化,而且在回流之后凝固形成的金属间化合物AuSn4较脆[1]。尽管如此,根据Lee和Chuang的研究[3],富Sn的金属间化合物有着适合用于封装应用的性能,而且它的使用将显著地减少材料的费用。
有若干种可以用于制备钎料薄膜的工艺,包括钎料预成型片、焊锡膏、物理沉积(气相沉积法或阴极真空喷镀法)以及电沉积。在这些工艺中,电沉积提供了经济效益及过程控制的最佳组合,尤其是对于钎料沉积在图样晶元而言[4]。根据目前所做的有限工作,这种富Sn化合物可通过气相沉积或通过源于两份分离的电解液中Au和Sn的连续电沉积制备而成[5-8]。连续电沉积的主要问题在于沉积物在从一种电解液转移到另一种电解液时会暴露于空气中。因为在空气中容易氧化,这种暴露对于Sn而言需特别关注。最近的一则出版物证实了富Sn的Au-Sn合金可以从一种单一电解液中沉积得到,这种单一电解液由Au和Sn的氯化物盐溶液组成,其中也含有硫酸钠、柠檬酸铵及其他添加剂[9]。可以通过改变电沉积条件尤其是电流密度而使成分在含~15wt%Sn到纯Sn范围内变化。
在此次研究中,采取了一种更为简便的方法来电沉积含有富Sn共晶合金的富Sn的Au-Sn钎料。使用的是作者早先研发的一种基于简单、绿色的Sn电镀液制成的单一电解液[10]。溶液中包含两种组分,氯化锡和柠檬酸铵,其保质期至少为3个月。可通过向溶液中添加Au颗粒而向其中加入Au,并因此形成一种悬浮液。使用悬浮的Au颗粒可以保持溶液纯净,因为其中只有一种物质会减少。此外,如果溶液中有相互竞争的物质,则会引起某一反应步骤为转移率所限制,那么沉积过程会变得难以控制。避免这些影响可以提高电解液的稳定性,并延长电镀槽的有效使用寿命。
图1 Au-Sn二元相图
- 实验过程
富Sn的Au-Sn合金钎料薄膜的电沉积可以在经过Ti/Au合金化的Si晶片上进行。其中Ti和Au都是溅射沉积得到的,Ti是作为Si以上的黏附层,而Au则是作为电沉积时的籽晶层。白金金属化的Si晶片被用作阳极。
用于制备沉积物的电化学电池体积为35ml,并提供了在水平方向上间距为1cm的电极。在沉积之前,悬浮液经过了5min的超声搅拌,以确保Au颗粒散开。在电沉积过程中,使用磁性搅拌棒来连续搅拌悬浮液。所有接通时间为2ms、停歇时间为8ms的脉冲电流条件下的沉积过程使用的都是一台Dynatronix DuPR 10-0.1-0.3 脉冲电镀电源。其平均电流密度在5至15mAcm-2范围内变化。
用于电沉积Sn的电镀溶液是一种简单、绿色的溶液,由氯化锡(SnCl42H2O浓度为50g/L)和柠檬酸三铵((NH4)3HC6H5O7浓度为75g/L)溶解于水得到,如[10]中所述。溶液的混合顺序很重要,柠檬酸三铵先加入水中,之后才添加氯化锡。当溶液澄清无色时混合完全。
图2 由HAuCl4盐制备的Au纳米颗粒的TEM选区衍射图案(a)和明视场图像(b)(TEM样品是通过向C覆盖的TEM栅格上放置一滴悬浮液并让液体蒸发而制备的)
Au-Sn悬浮液可以通过两种方法制备得到。于第一种方法而言,在参考文献[11]中叙述的步骤后便可接着制备分离的Au纳米颗粒悬浮液。首先,通过将0.1gHAuCl4溶于500ml蒸馏水得到一份溶液。然后通过向50ml蒸馏水中加入0.5g柠檬酸钠(Na3C6H5O7)制备得到另一份溶液。HAuCl4溶液需加热至沸腾,届时再将柠檬酸钠溶液缓慢加入HAuCl4溶液中。通过加水使溶液体积保持在500ml。当溶液变为深红色时Au纳米颗粒悬浮液便已制备完成。在使用前需将悬浮液冷却至室温。利用透射电子显微镜(TEM)证实(图2)可得悬浮液中的Au颗粒非常稳定而且尺寸均一(10-20nm)。悬浮液的稳定性可以归因于柠檬酸阴离子(源于柠檬酸钠)覆盖了Au纳米颗粒的表面并且产生静电排斥从而避免颗粒间的凝聚以及从溶液中沉降分离[11]。
形成电解液时,最初氯化锡和柠檬酸盐是直接加入Au纳米颗粒的悬浮液中的;然而,Au纳米颗粒会变得不稳定。柠檬酸离子覆盖层从颗粒表面剥离进而导致颗粒之间的斥力消除[11],从而引起团聚。因此,之后的电解液是通过混合Au纳米颗粒悬浮液和Sn的柠檬酸盐溶液而制备的。可以通过在混合前蒸发纳米颗粒悬浮液中的一些水而改变电解液中Au的数量。
在第二种方法中,Au颗粒(尺寸为500-800nm)被直接加入柠檬酸锡溶液中。加入的量在0.5至1.0g/L内变化。通过使用扫描电子显微镜(SEM——在本章节内稍后再做描述)证实了Au颗粒的大小。部分颗粒的二次电子(SE)照片如图3a.所示。X射线能谱仪(EDX)微量分析证实颗粒物确实是纯Au。X射线光电子能谱仪(XPS)显示颗粒物被有机涂层所覆盖,这可能有助于避免凝聚。进行XPS分析时,使用了Kratos AXIS 165 XPS系统,光源为单色Al的Kalpha;,电流大小为15mA。探测图谱是使用160eV的电压来得到的,高分辨率光谱则是利用20eV的电压来得到。图3b中的XPS光谱显示了Au的最强峰以及源于C,O,N的峰。至少有一部分C的峰可以归因于表面污染,但是N的峰并不是污染的特征。Au颗粒的供应商(Sigma-Aldrich)证实了颗粒物被专用的有机层所覆盖。
选择沉积后的物品置于室温空气中持续2周进行时效处理,以研究Au颗粒和Sn基体间的互相扩散。另有几个样品被置于混合气体氛围(5%H2-95%N2)中的一个封闭的热板炉内,在235至250℃间进行回流。
沉积、失效及退火处理过的样品是通过Hitachi H2700 SEM进行检测的,工作时的电压为20KV并且配备了PGT IMIX超窄窗口X射线能谱(EDX)探测器。通过三个不同区域的平均EDX分析可鉴定沉积组成物,各区域大小约为300mu;m见方。切断后用环氧树脂固定再用SiC砂纸打磨然后用硅胶抛光可制成截面分析所需样品。
图3 a为Au颗粒的SEM二次电子(SE)照片,b为亚微米Au颗粒的XPS探测图谱
-
结果与讨论
- 使用Au纳米颗粒悬浮液的电沉积
通过混合Au纳米颗粒悬浮液和Sn溶液可以制备用于每一个单独的电镀过程的新鲜电解液。通过控制混合前Au纳米颗粒悬浮液中水的蒸发可使电解液中Sn:Au质量比在250至50内变化。如果沉积物浓度和电解液浓度一致,则会生成Au含量在0.4至2.0wt%范围内变化的沉积物,这也和Au-Sn相图(图1)中过共晶的一侧相符。在所有情况下,沉积物都表现出不良的形貌,也即多孔且在侧向和垂直方向上都不均一。不同Sn:Au质量比的电解液对应的俯视图和截面图示例如图4所示。沉积物中含有Au,但由于表面粗糙,其数量利用EDX分析难以精确衡量。一般沉积物中Au的含量会随着电解液中Au含量的增加而增加,其成分在~1wt%至~5wt%范围内变化。这一数量要比电解液中Au的相对含量高。
通过改变电解液制备的方法可尝试改善沉积物的形貌。电解液中过量的柠檬酸离子可能与沉积物的不良形貌有关。因此,制备电解液时直接向Au悬浮液(不添加柠檬酸铵)中加入Sn盐。加入氯化锡时,Au纳米颗粒立即团聚并沉降至容器底部。Au的团聚表明没有充足的柠檬酸离子在与Sn络合的同时使悬浮液中的Au稳定。事实上,Sn很可能剥夺了Au颗粒物的柠檬酸覆盖层。对颗粒物用超声波处理使其分散并使用7.5mAcm-2的平均电流密度制备沉积物。得到的这些沉积物的形貌比图4中的甚至更差,并且其中还含有松散分布的岛状Sn(本文中未显示)。
图4 由通过混合柠檬酸锡溶液和Au纳米颗粒悬浮液制备的电解液得到的Sn-Au沉积物的SEM SE照片(平面和横截面),a和b对应的电解液中Sn:An的质量比等于250,c和d对应的电解液中Sn:Au的质量比等于125,e和f对应的电解液中Sn:Au的质量比等于50(所有的沉积物都在平均电流密度为7.5mAcm-2、占空比为20%的条件下获得)
将Sn溶液中柠檬酸离子的来源从柠檬酸铵变为柠檬酸钠。柠檬酸钠与Au纳米颗粒悬浮液制备过程中所用的添加剂相同。加入的柠檬酸钠的量需调整至所含柠檬酸离子浓度和氯化锡—柠檬酸铵溶液相同。然而,因为Au颗粒发生团聚且从悬浮液中分离出来,所以产生的电解液并不稳定。如上一段所述,团聚的颗粒物在电沉积前经过了超声波的分散处理。最终得到的沉积物展现出了不良的形貌(本文中未显示)。
总而言之,由氯化锡—柠檬酸铵溶液和Au纳米颗粒悬浮液(含有柠檬酸钠)组成的电解液可以制得富Sn的Au-Sn沉积物,然而沉积物孔隙度高且不均匀地分布在基片表面上。因此,需选择另一种替代方法,以粉末形式将Au颗粒直接加入氯化锡—柠檬酸铵溶液中。
图5 由Sn溶液得到的电沉积物的SEM SE平面(a)和横截面(b)照片(由Sn溶液和Au颗粒悬浮液(1.0g/L)的混合物得到的电沉积物的SEM SE平面(a)和横截面(b)照片,两份沉积物均在电流密度为10mAcm-2且持续60分钟的条件下制备)
-
- 使用Au粉末(尺寸为500-800nm的颗粒)的电沉积
在Au颗粒含量为1.0g/L、电流密度为10mAcm-2且持续一小时的条件下使用简单Sn溶液和Au颗粒组成的悬浮液初步尝试将Au颗粒混入Sn沉积物中。两份沉积物的SEM SE照片如图5所示,其中一份是来自Sn溶液,另一份则来自Sn溶液与Au纳米颗粒悬浮液的混合物。两份沉积物都是连续的而且相对光滑,并且Au颗粒很明显地混入了Sn沉积物中(图5c,d)。亚微米的Au颗粒并未影响沉积物形貌;然而,沉积速率从纯Sn沉积时的约20mu;mhr-1降到Au-Sn沉积时的约15mu;mhr-1。
图6 使用不同电流密度制备的Au-Sn沉积物的平面及横截面的SEM SE图像,a和b对应5mAcm-2,c和d对应7.5 mAcm-2,e和f对应10 mAcm-2,g和h对应15 mAcm-2(所有沉积物都是由含有1.0g/LAu颗粒的悬浮液获得的,且沉积时间为1h)
-
-
-
- 电流密度的影响
-
-
悬浮液中的颗粒含量及沉积时间分别保持在1.0g/L及1h,同时电流密度在5至15mAcm-2内变化。为了确保电流密度是唯一变量,每一次沉积都制备了一份新鲜的Sn溶液及Sn/
剩余内容已隐藏,支付完成后下载完整资料
资料编号:[137159],资料为PDF文档或Word文档,PDF文档可免费转换为Word
课题毕业论文、外文翻译、任务书、文献综述、开题报告、程序设计、图纸设计等资料可联系客服协助查找。